近日,Jasper Therapeutics公司宣布,裁员50%,并暂停其他临床以及临床前项目,以集中资源用于其核心管线Briquilimab在慢性荨麻疹的临床开发。
这一重组计划正由两天前,Briquilimab的一项Ⅰb/Ⅱa期临床BEACON数据引发,两天前,Jasper报告,因为Briquilimab“生产批次”问题,导致该试验中两个多剂量组的临床表现不及预期。最终,Jasper直接宣布终止其针对哮喘以及严重联合免疫缺陷症的临床开发,并计划采取削减成本措施。
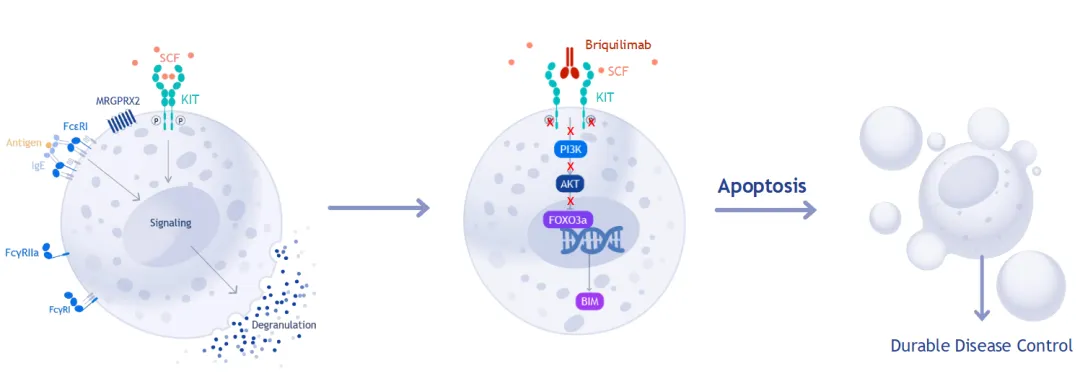
Briquilimab是一款靶向KIT(CD117)的单克隆抗体,通过阻断干细胞因子(SCF)与细胞表明受体KIT结合,诱导肥大细胞凋亡。两天前(7月7日),Jasper刚刚公布了Briquilimab一项Ⅰb/Ⅱa期临床BEACON数据,用于治疗慢性自发性荨麻疹(CSU)。试验结果显示,240mg单剂量组中,100%的患者实现了完全缓解(UAS7=0),UAS7(7天荨麻疹活动评分)较基线平均下降了28.3分。360mg单剂量组中,75%的患者实现了完全缓解,UAS7较基线平均下降了22.9分。Briquilimab的耐受性良好,没有报告3级或更高级别的治疗相关不良事件,也没有观察到剂量限制性毒性。然而,该试验中两个多剂量组—240mg(8周)、240mg(8周)→180mg(8周)的临床结果令人较为失望,其中10名患者的平均胰蛋白酶水平降幅均低于预期且UAS7评分没有显著改善。而据该公司称,导致这一问题的原因是生产批次问题,有10名患者均使用了问题“产品批次”,而同属该剂量组的两名被证实使用不同“产品批次”的患者则实现了完全缓解。受影响还有哮喘,这一问题“批次产品批次”也被用于一项针对哮喘的临床试验。
Jasper表示,正在试验站点提供新批次药品,并调查导致”问题产品批次“产生的原因,同时,因为这一”产品批次“问题,公司决定终止Briquilimab在哮喘以及针对严重联合免疫缺陷症的开发。
仅仅是因为出现”生产批次“问题便进行裁员重组,这一理由似乎说不过去。
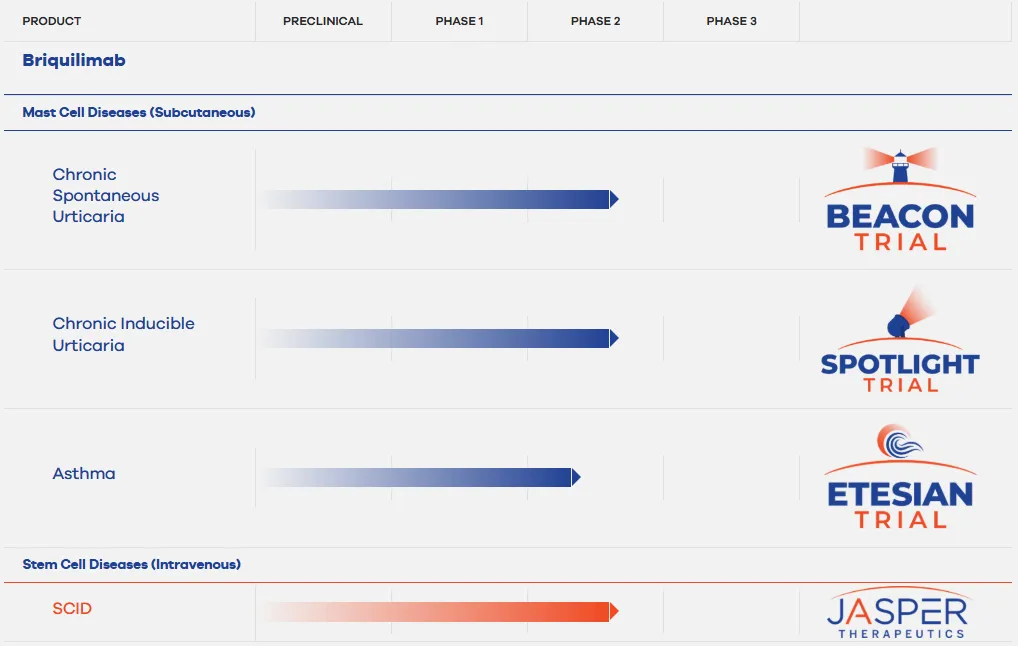
Briquilimab是Jasper的目前唯一的管线,其开发了慢性自发性荨麻疹(CSU)、慢性诱导性荨麻疹(CIndU)、哮喘、严重联合免疫缺陷症等多个适应症。被放弃的哮喘、严重联合免疫缺陷症都已经推进到临床Ⅱ期阶段。就公司的财务情况来看,即便不是出现生产批次的问题,公司也需要采取成本削减措施。截至2025年3月31日,公司现金及其等价物仅有4880万美元,净亏损2120万美元。此次裁员重组是为了延长现金流,但Jasper并未披露可以延长公司现金跑道到何时。
*声明:本文内容转载于网络,版权归原作者所有,转载目的在于传递信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除!
(https://mp.weixin.qq.com/s/kSf0twMENX0ss180fomUnw)