ЛЖгФњзЂВсЦбЙЋгЂ
ФњашвЊ ЕЧТМ ВХПЩвдЯТдиЛђВщПДЃЌУЛгаеЪКХЃПСЂМДзЂВс
x
вРППDNAЫ№ЩЫгеЕМРДИљГ§КЭвжжЦАЉЯИАћЩњГЄЕФВпТдЪЧАЉжЂжЮСЦЕФећЬхЗНАИЁЃвђДЫЃЌЦЦвыDNAЫ№ЩЫЗДгІЃЈDDRЃЉЖдАЉжЂЕФжЮСЦжСЙиживЊЁЃНёЬьЃЌОЭШУаЁЬеХуФувЛЭЌСЫНтЁАЛљвђЮРЪПЁБp53гыDNAЫ№ЩЫЗДгІжЎМфЕФФЧаЉЪТЖљ~ P53 ЪЧвЛжжжзСівжжЦЕААзКЭзЊТМвђзгЃЌПЩЕїПиЯИАћЗжСбЃЌзшжЙ DNA ЭЛБфЛђЪмЫ№ЕФЯИАћНјааЗжСбВЂЭЈЙ§зЊТМЕїПиЯђетаЉЯИАћДЋЕМЕђЭіаХКХЃЌДгЖјзшжЙжзСіаЮГЩЁЃ
ЫќПЩвдЖдЯИАћгІМЄЛђ DNA Ы№ЩЫзїГіЯьгІЃЌМЄЛюЖржжзЊТМАаБъЁЃp53 ЛЙПЩаЕїЖржжЗДгІЃЌАќРЈЯИАћжмЦкзшжЭЁЂDNA аоИДЁЂДњаЛИФБфЁЂПЙбѕЛЏзїгУЁЂПЙбЊЙмЩњГЩзїгУЁЂздЪЩЁЂЫЅРЯКЭЕђЭіЁЃp53 гы DNA Ы№ЩЫЗДгІЕФЁАвЛЩњЁБвВзЂЖЈЛсОРВјВЛЖЯ......
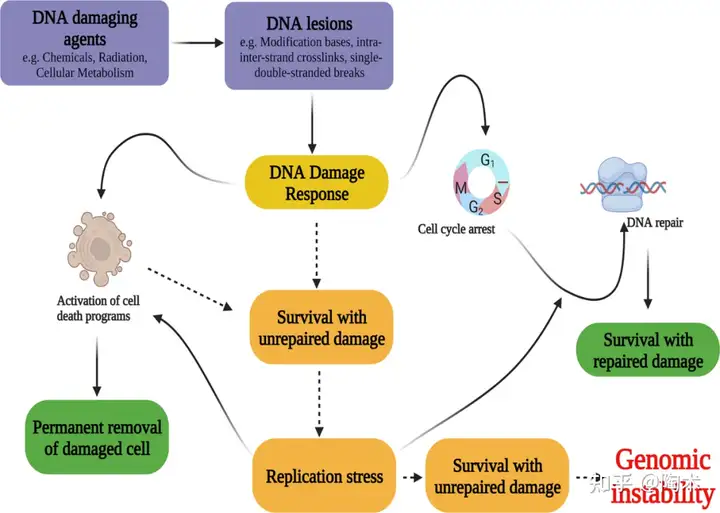
ЁјDNAЫ№ЩЫЗДгІЭјТч2022Фъ10дТ8ШеЃЌЗЂБэгк Experimental & Molecular Medicine ЕФвЛЦЊзлЪібаОПСЫжзСівжжЦвђзг p53 МвзхдкАЉжЂжаЕФЕїНкЭјТчЁЃЧПЕїСЫ UBE4B ПЩФмдкЯИАћЖд DNA Ы№ЩЫЕФжїЖЏЗДгІжаЗЂЛгживЊзїгУЃЌВЂВћЪіСЫ p53 ЕїНкМСЃЌЕААзМЄУИКЭ E3 / E4 ЗКЫиСЌНгУИМАЦфПЙАЉЧБСІЁЃ  баОПЗЂЯжСзЫсЛЏЕФ p53 жївЊЭЈЙ§Цфгы HDM2 КЭ UBE4B ЕФНтРыЖјЮШЖЈЃЛВЂЧв p53 ЕААзЛсЛ§РлВЂзЊвЦЕНЯИАћКЫжаЁЃдкЯИАћКЫжаЃЌp53 ОлМЏЮЊЫФОлЬхЃЌМД p53 ЕФЛюадаЮЪНЃЌВЂзЊТММЄЛюЛђвжжЦЦфАаЯђЛљвђЃЌАќРЈЯИАћжмЦкЕААзвРРЕадМЄУИвжжЦМС p21 КЭдЕђЭіЛљвђ Puma КЭ BaxЁЃ СзЫсЛЏЕФ p53 ЭЈЙ§ИКЗДРЁЛиТЗзЊТМгеЕМЦфДѓЖрЪ§ИКЕїНквђзгЃЌАќРЈ HDM2ЃЌUBE4B КЭ Wip1ЁЃвЛЕЉ DNA Ы№ЩЫЕУЕННтОіЛђВЛашвЊ p53 ЛюадЃЌp53 МАЦфДѓЖрЪ§ИККЭе§ЕїНкМСЭЈЙ§ Wip1 НјааШЅСзЫсЛЏЁЃДЫЭтЃЌUBE4B НсКЯВЂНЕНтСзЫсЛЏЕФ p53ЃЌВЂЧв UBE4B дкЯьгІЕчРыЗјЩфЪБЖРСЂИКЕїСзЫсЛЏ p53ЁЃ ЕЋ p53 гы DDR жЎМфЕФЙиЯЕЛЙвЊИќМгЕФИДдг......
P53ЕФЕїПи
дк DNA Ы№ЩЫЙ§ГЬжаЃЌp53 ОРњИДдгЕФЗвыКѓаоЪЮзїгУЃЈPTMЃЉЃЌАќРЈЗКЫиЛЏЁЂввѕЃЛЏЁЂМзЛљЛЏКЭ SUMOЃЈsmall ubiquitin-related modifierЃЉЛЏЕШЃЌ ВЂЧвВЛЭЌЕФ PTM ЯрЛЅНјааДЎШХКЭЯрЛЅзїгУЃЌвдЬиЖЈЕФЗНЪНгааЇКЭОЋШЗЕижИЕМ p53 ЛюЖЏЁЃЯТУцЮвУЧМђЕЅНщЩмвЛЯТЦфжївЊЕїНкЭООЖЁЃ 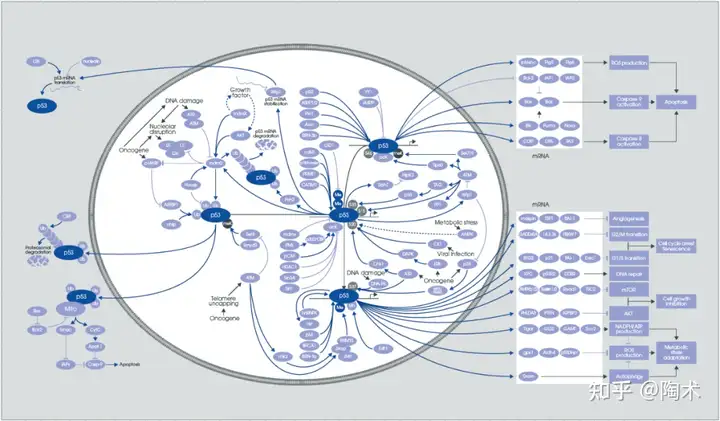
ЁјP53аХКХЭЈТЗЁЃ- ATM-CHK2 КЭ ATR-CHK1 ЪЧ p53 ЛюадЕФжївЊЕїНкЭООЖЃЌвдЯьгІЖржжРраЭЕФ DNA Ы№ЩЫ
ЮЊЯьгІЯИАћгІМЄЃЌp53 ПЩБЛПьЫйМЄЛюЃЌВЂЭЈЙ§вЛЯЕСа PTM зїгУДІгкЮШЖЈзДЬЌЁЃp53 ЕФгеЕМКЭМЄЛюжївЊгЩУЋЯИбЊЙмРЉеХадЙВМУЪЇЕїЭЛБфЛљвђЃЈATMЃЉКЭУЋЯИбЊЙмРЉеХадЙВМУЪЇЕїЯрЙиЛљвђЃЈATRЃЉНщЕМЁЃ ATM жївЊдкЫЋСД DNA Ы№ЩЫЪБЗЂЛгЁАМрВтЕуЁБзїгУЃЛATR дђИКд№ИагІВЂДЋЕНЦфЫћаЮЪНЕФ DNA Ы№ЩЫЃЌЫќУЧЯрЖдЖРСЂЖјгжЯрЛЅНЛЭЈЃЌЙВЭЌМЄЛюЯТгЮФПЕФЕААзШч CHK1ЃЈМрВтЕуМЄУИ1ЃЉЁЂCHK2ЃЈМрВтЕуМЄУИ2ЃЉМА p53 ЭЈТЗЕААзЕШЗЂЛгзїгУЁЃ DNA ЫЋСДЖЯСбЃЈDSBЃЉЛсЕМжТ ATM МЄЛюЃЌЛюЛЏЕФ ATM ФмСзЫсЛЏвЛЯЕСаЕзЮяЗжзгЃЌЦфЫћаЮЪНЕФ DNA Ы№ЩЫдђЛсзюжеЕМжТ ATR ЕФМЄЛюЁЃетСНИіМЄУИ DNA Ы№ЩЫМЄЛюКѓЃЌЗжБ№СзЫсЛЏЯТгЮЕзЮяШч CHK1ЁЂCHK2ЁЂp53 ЕШЃЌЖј p53 зїЮЊ DNA Ы№ЩЫаХКХЭјТчжаЕФЁАЗжзгНкЕуЁБЃЌИКд№ЁАаХКХЁБЕФМЏжаМАОіЖЈЫ№ЩЫаЇгІЫљЕМжТЕФЯИАћЕФзюжеУќдЫЁЃ ЫфШЛ ATM-CHK2 КЭ ATR-CHK1 ЭЈТЗЖдВЛЭЌРраЭЕФЫ№ЩЫгаЗДгІЃЌЕЋЫќУЧЕФзїгУЪЧжиЕўЕФЃЌВЂЧвЫќУЧЕФаЭЌЗДгІдкЯьгІВЛЭЌЕФ DNA Ы№ЩЫвђзгЪБЯрЛЅВЙГЅЁЃ злЩЯЫљЪіЃЌATM-CHK2 КЭ ATR-CHK1 ЪЧжааФМЄУИЃЌПЩВЛЖЯСзЫсЛЏ p53 МАЦфИКЕїНквђзгЃЈШч MDM2ЁЂMDM4ЁЂCop1 КЭ Trim24ЃЉЃЌвдгІЖдВЛЭЌРраЭЕФЯИАћгІМЄКЭ DNA Ы№ЩЫЁЃ
MDM2 ЪЧИКд№вАЩњаЭЯИАћжа p53 НЕНтЕФ E3 ЗКЫиСЌНгУИЃЌПЩЭЈЙ§СНжжаЮЪНЕїНк P53 ЙІФмЃКЂйMDM2 НщЕМ p53 ДЉЙ§КЫФЄНјШыАћНЌНЕНтЁЃp53 ЕФНЕНтЛсгАЯь MDM2 ЛљвђзЊТМЃЌНЋ p53-MDM2 ИКЗДРЁЛЗТЗЙиБеЃЛЂкMDM2 Жд P53 зЊТМЛюадЕФжБНгвжжЦзїгУЁЃ Г§СЫЖд p53 ЕААзЕФжБНгзїгУЭтЃЌMDM2 ЛЙПЩЭЈЙ§гАЯь p53 ЕФЗвыгАЯьЦфЙІФмЃЌЦфжївЊгаСНжжЛњжЦЃКЂйЭЈЙ§гы mRNA жБНгзїгУЃЌгАЯь p53 ЕФЗвыЃЛЂкЖЈЯђзїгУгђКЫЬЧЬхЕААз RPL26ЃЌЕМжТЦфЗКЫиЛЏНЕНтЃЌЕБ DNA Ы№ЩЫЪБетжжзїгУЛсБЛвжжЦЃЌДгЖјЪЙЕУ p53 ЕФ mRNA ПЩвдЭЈЙ§ RPL26 НјааЗвыЁЃ вђДЫЃЌMDM2-p53 ЯрЛЅзїгУГЩЮЊАЉжЂжЮСЦЕФЙиМќАаБъЁЃ
P53ЕФАаЯђжЮСЦ
жзСівжжЦвђзг p53 ДІгк DNA Ы№ЩЫЗДгІЕФжааФЁЃPTM жївЊЕїНк p53 ЛюадвдЯьгІ DNA Ы№ЩЫЁЃАаЯђ PTM геЕМЕФ p53 ЕїНкМСвбОдкЪЕбщЪвКЭСйДВЛЗОГжаБЛжЄУїПЩвдЪЙАЉЯИАћЖд DNA Ы№ЩЫМСУєИаЁЃМИжжАаЯђ p53 ЛюадИКЕїПивђзгЕФаЁЗжзгвжжЦМСвбБЛЙуЗКгІгУгкЗХЩфКЭЛЏСЦСЊКЯжЮСЦЁЃЦфжааэЖрвжжЦМСФПЧАДІгкСйДВЪдбщНзЖЮЁЃ 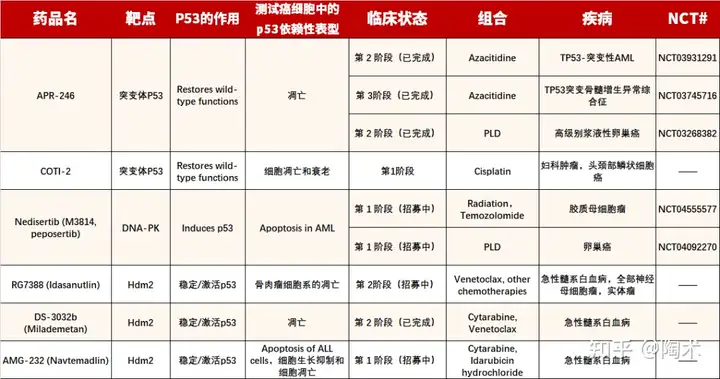 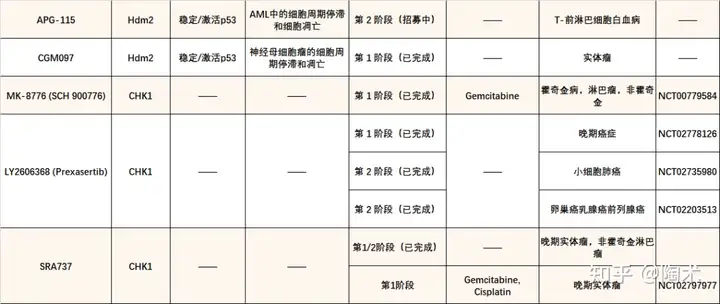 Г§ДЫжЎЭтЃЌгкНёФъ 10 дТ 10 ШеЗЂБэгк Nature Reviews Drug Discovery ЩЯЕФвЛЦЊзлЪіЛЙЖдАаЯђ p53 ЕФВЛЭЌЪжЖЮНјааСЫХЬЕуЁЃДгДЋЭГЕФаЁЗжзгвЉЮяЃЌЕНЫЋЬивьадПЙЬхЁЂЕААзНЕНтСЦЗЈЁЂЛљвђСЦЗЈКЭ RNA СЦЗЈЕШДДаТжЮСЦФЃЪНЖМгаЩцМАЁЃ  ЖдетЗНУцЕФЭЛЦЦадЕФНјеЙВЛНіЖдгкРэНтжзСіЗЂЩњЗЂеЙЕФВЁРэЛњжЦгазХживЊзїгУЃЌЭЌЪБПЩвдЮЊПЙжзСівЉЮяПЊЗЂКЭгІгУЬсЙЉживЊЕФРэТлвРОнЁЃ ЙизЂЙЋжкКХЃКЬеЪѕЩњЮя СЫНтИќЖрЧАбизЪбЖ~ ЙизЂЪгЦЕКХЁЂпйСЈпйСЈЃКЬеЪѕаЁПЮЬУЃЌбЇЯАИќЖрOPENEyeЃЌHTSЃЌвЉЩИжЊЪЖИЩЛѕ~ ВЮПМзЪСЯ [1] Abuetabh, Y., Wu, H.H., Chai, C. et al. DNA damage response revisited: the p53 family and its regulators provide endless cancer therapy opportunities. Exp Mol Med (2022). https://doi.org/10.1038/s12276-022-00863-4 [2] Wang YJ, Sun H, Liu GT, Chen XG. [Advances in the study of p53 in response to DNA damage]. Yao Xue Xue Bao. 2011 Dec;46(12):1413-9. Chinese. PMID: 22375412. [3] Hassin and Oren, (2022). Drugging p53 in cancer: one protein, many targets. Nature Reviews Drug Discovery, https://doi.org/10.1038/s41573-022-00571-8 [4] Xiao et al., (2022). Combining p53 mRNA nanotherapy with immune checkpoint blockade reprograms the immune microenvironment for effective cancer therapy. Nature Communications, https://doi.org/10.1038/s41467-
|  |ЪжЛњАц|ЦбЙЋгЂ|ouryao|ЦбЙЋгЂ
( ОЉICPБИ14042168КХ-1 ) діжЕЕчаХвЕЮёОгЊаэПЩжЄБрКХЃКОЉB2-20243455 ЛЅСЊЭјвЉЦЗаХЯЂЗўЮёзЪИёжЄЪщБрКХЃК(ОЉ)-ЗЧОгЊад-2024-0033
|ЪжЛњАц|ЦбЙЋгЂ|ouryao|ЦбЙЋгЂ
( ОЉICPБИ14042168КХ-1 ) діжЕЕчаХвЕЮёОгЊаэПЩжЄБрКХЃКОЉB2-20243455 ЛЅСЊЭјвЉЦЗаХЯЂЗўЮёзЪИёжЄЪщБрКХЃК(ОЉ)-ЗЧОгЊад-2024-0033