欢迎您注册蒲公英
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
一、分类和标准
从生产技术角度,目前市面上的口罩基本分为三类:日常防护型口罩、专业呼吸防护口罩以及医用口罩。
第一种,日常防护型口罩,主要指日常生活中,空气污染环境下滤除颗粒物所佩戴的防护型口罩,执GB32610-2016《日常防护型口罩技术规范》,要求佩戴各防护等级口罩后使吸入的PM2.5浓度降低至75微克每立方米以下,即过滤后吸入体内的空气质量达到良及以上水平,才是合格的日常用防护口罩。第二种,专业防护口罩,执行GB2626—2006《呼吸防护用品——自吸过滤式防颗粒物呼吸器》, 此标准主要针对安全环保,防护对象从粉尘到各类颗粒物,包括粉尘、烟、雾和微生物。第三种,医用防护口罩,又分医用防护口罩、医用外科口罩和一次性使用医用口罩。(1)医用防护口罩适用于医务人员和相关工作人员对经空气传播的呼吸道传染病的防护。(2)医用外科口罩适用于医务人员或相关人员的基本防护,以及在有创操作过程中阻止体液和喷溅物传播的防护。(3)一次性使用医用口罩适用于佩戴者在不存在体液和喷溅风险的普通医疗环境下的卫生护理。三种医用口罩执行标准如下:(1)医用防护口罩:应符合GB 19083-2010《医用防护口罩技术要求》;(2)医用外科口罩:应符合YY 0469-2011《医用外科口罩》;(3)一次性使用医用口罩:应符合YY/T 0969-2013《一次性使用医用口罩》要求。
二、法规要求及检测要求
2019年01月15日的“国家药监局持续推进医疗器械注册技术审查指导原则制修订工作 ”中指导原则附录第47条为“医用口罩产品注册技术审查指导原则”。该指导原则适用于医用防护口罩、医用外科口罩和医用普通口罩(一次性使用医用口罩)。经查,医用口罩归属于《医疗器械分类目录》中管理类别为Ⅱ类,6864(医用卫生材料及敷料类),因此必须取得药品监督管理局颁发的注册证方可销售,监管比较严格。
(一) 医用口罩生产原料及分类常见的医用口罩主要由三层无纺布组成,内层是普通无纺布,外层是做了防水处理的无纺布,主要用于隔绝患者喷出的液体,中间一层是主体过滤材料,常用聚丙烯熔喷布材料。口罩生产用到的其他材料还包括,金属(用于鼻夹)、弹性材料(用于口罩带)等。医用口罩按照面罩形状可以分为平面形、鸭嘴形、拱形或折叠式等。按照佩戴方式可以分为耳挂式、绑带式或头带式。(二) 医用口罩的检测要求(1)医用口罩产品的检测包括出厂检验和型式检验。(2)出厂检验项目至少应有以下项目:外观、结构与尺寸、鼻夹、口罩带、微生物指标、环氧乙烷残留量(若采用环氧乙烷灭菌)的要求。(3)型式检验应为产品标准的全性能检验。(4)生物相容性检测。以下部分(第三部分、第四部分)仅对医用防护口罩相关内容(执行GB 19083-2010《医用防护口罩技术要求》)作一阐述。
三、生产工艺流程
口罩成型→压合→切边→呼吸阀焊接→耳带点焊→鼻梁条线贴合→呼吸阀冲孔→包装→灭菌→解析(EO灭菌)→成品
全自动化机器相对来说省时高效,原材料挂于料架上,机台自动送料,由1台本体机拖2到3台耳带机进行自动生产。
四、生产环境与主要生产设备
(一)医药防护口罩生产环境
医用防护口罩执行GB 19083-2010《医用防护口罩技术要求》,包装上有灭菌或者无菌字样的口罩应无菌,按要求执行YY 0033-2000 《无菌医疗器具生产管理规范》。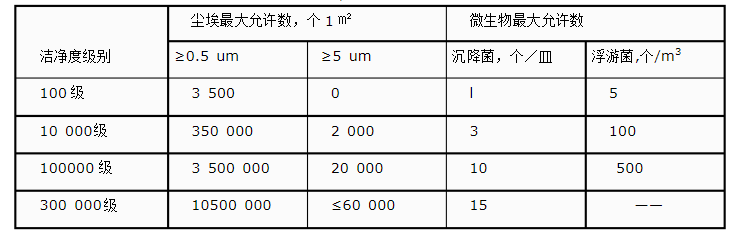
图1无菌医疗器具洁净室空气洁净度级别表(附录A)附录B无菌医疗器具产品生产环境洁净度级别设置指南中明确:B4(B3规定以外的)无菌医疗器具或单包装出厂的零部件(不清洗件)的加工、末道精洗、组装、初包装及其封口均应在不低于300 000级洁净室(区)内进行。参照附录B,医用防护口罩生产一般在10万级洁净车间生产。(二)医药防护口罩主要生产设备1.口罩生产设备医用防护口罩口罩的生产一般是全自动或者半自动设备。半自动的设备包括口罩成型机、口罩压合机、口罩切边机、呼吸阀冲孔机(若有呼吸阀)、鼻梁条线贴合机、耳带点焊机、呼吸阀焊接机(若有呼吸阀);全自动设备包括全自动平面口罩机、全自动折叠口罩机等,费用较高但省时高效。2.灭菌设备生产无菌医用口罩,涉及到灭菌工序。目前绝大部分企业选择的是环氧乙烷(EO)灭菌设备。环氧乙烷灭菌的口罩需要进行解析。因为环氧乙烷灭菌后,口罩上会有环氧乙烷残留,而环氧乙烷是一种有毒的致癌物质,长期吸入环氧乙烷,不但刺激呼吸道,还会有致癌可能性。长期少量接触,可见有神经衰弱综合征和植物神经功能紊乱。因此,经环氧乙烷灭菌的医用口罩,必须经过解析释放口罩上残留的环氧乙烷,经检测合格才能出厂上市。经过验证的环氧乙烷解析时间约为14天,可确保口罩中残留的环氧乙烷含量低于10ug/g的安全标准。 另外,环氧乙烷灭菌的口罩应选用透气的内包装材料。否则环氧乙烷难以穿透,难以达到灭菌效果。以上从口罩分类、医用口罩管理办法及生产技术要求、生产工艺流程、生产环境与主要生产设备四方面对医用防护口罩生产线建设相关问题做了汇总,以便于疫情期间同行交流参考。
五、口罩注册需要的资料
1.应急备案资料(应急防疫用,一般是1年内有效期) 1、企业营业执照副本复印件 2、产品技术要求(三份) 3、说明书、标签样稿 4、该产品实物样照片; 5、企业与原材料供应商签订的购货合同; 6、企业自检报告; 7、企业委托当地药品检验机构进行微生物检验或无菌检验的报告(如有); 8、企业承诺书(包括:产品质量安全承诺,资料真实性的自我保证声明)。
2.普通注册申请资料(5年有效期) 1、申请表 2、证明性文件; 3、医疗器械安全有效基本要求清单; 4、综述资料; 5、研究资料; 6、生产制造信息; 7、临床评价资料; 8、产品风险分析资料; 9、产品技术要求一式两份; 10、产品注册检验报告; 11、产品说明书一式两份; 12、最小销售单元的标签样稿; 13、符合性声明及自我保证声明; 14、企业认为需要申报的其他文件资料。
六、口罩注册周期
1.应急审批注册周期(部分药监局已缩短流程,以当地药监局为准) 首先,确定为应急医疗器械产品的企业需递交注册申报资料,相应医疗器械注册受理部门受理后,将该注册申请项目标记为"应急审批",并于受理当日由专人负责进行注册申报资料流转。 其次,第二类应急审批医疗器械注册申请受理后,药品监督管理部门应当在5日内完成技术审评;技术审评结束后,在3日内完成行政审批。 同时,第三类应急审批医疗器械注册申请受理后,药品监督管理部门应当在10日内完成技术审评;技术审评结束后,在3日内完成行政审批。 再次,对于应急审批医疗器械,相关医疗器械检测机构应当在接收样品后24小时内组织开展医疗器械注册检测,并及时出具检测报告。 然后,对于应急审批医疗器械,相应的药品监督管理部门在接到生产企业质量管理体系考核申请后,应当在2日内组织开展现场考核工作,并及时出具质量管理体系考核报告。
2.普通注册周期(工作日)
二类:受理3+资料转移5+技术审批60+审批20+制证发证10(总计98个工作日,部分药监局已缩短流程,以当地药监局为准,不含发补周期)三类:受理3+资料转移5+技术审批90+审批20+制证发证10)(不含发补周期)
|  |手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033
|手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033